CuO phản ứng với 2HCl là một phản ứng hóa học phổ biến, thường được sử dụng trong các thí nghiệm hóa học cơ bản. Phản ứng này cho thấy rõ sự tương tác giữa một oxit bazơ (CuO) và một axit (HCl), tạo ra muối và nước. Hiện tượng quan sát được là chất rắn màu đen CuO tan dần trong dung dịch HCl không màu, tạo thành dung dịch màu xanh lam của CuCl2.
Phản ứng hóa học giữa CuO và 2HCl
Phản ứng giữa CuO và 2HCl được biểu diễn bằng phương trình hóa học sau:
CuO(r) + 2HCl(aq) → CuCl2(aq) + H2O(l)Trong đó:
- CuO (r): Đồng(II) oxit (chất rắn)
- HCl (aq): Axit clohydric (dung dịch)
- CuCl2 (aq): Đồng(II) clorua (dung dịch)
- H2O (l): Nước (lỏng)
Phản ứng này thuộc loại phản ứng trao đổi, cụ thể là phản ứng trung hòa giữa oxit bazơ và axit.
Hiện tượng quan sát được khi CuO tác dụng với 2HCl
Khi cho CuO vào dung dịch HCl, ta sẽ quan sát thấy:
- Chất rắn màu đen CuO tan dần.
- Dung dịch chuyển từ không màu sang màu xanh lam đặc trưng của ion Cu2+.
Đây là dấu hiệu cho thấy phản ứng hóa học đã xảy ra và tạo thành sản phẩm mới là CuCl2.
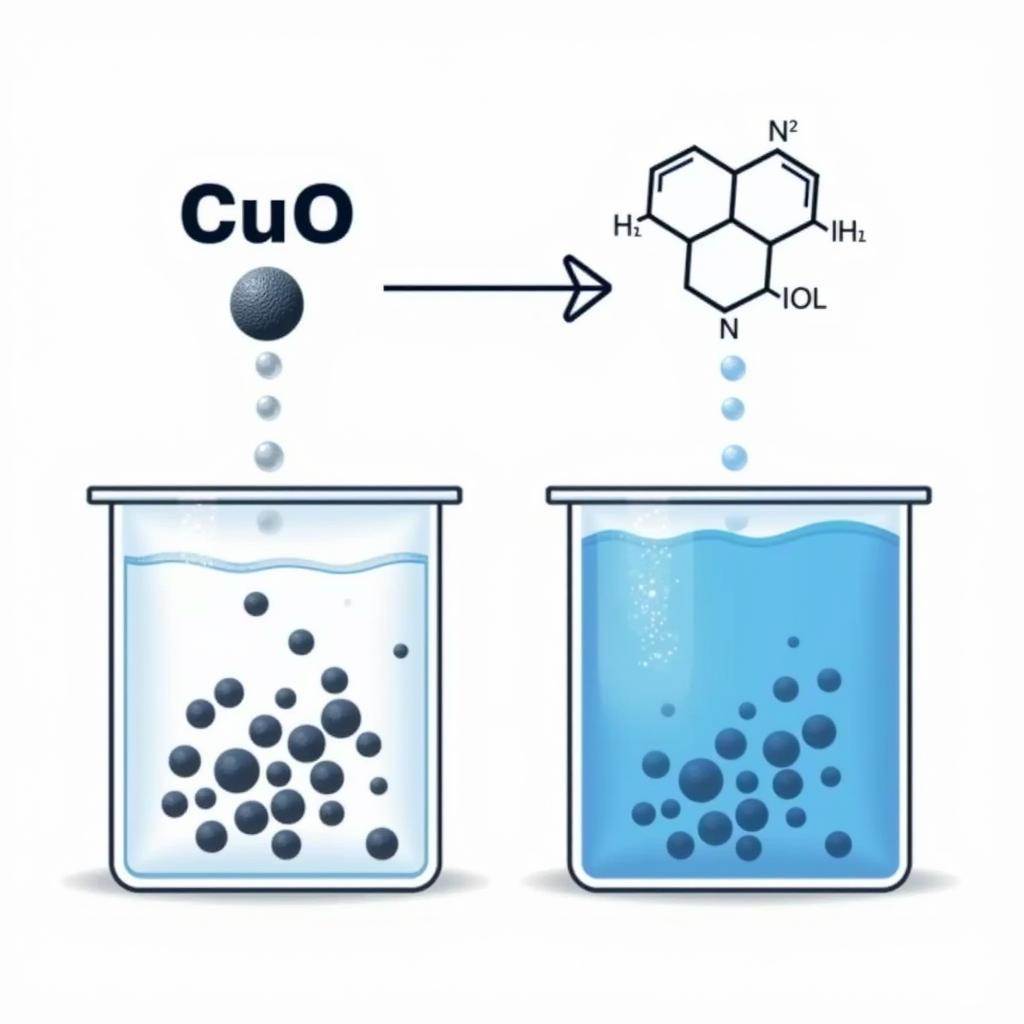 Phản ứng giữa CuO và 2HCl
Phản ứng giữa CuO và 2HCl
Tại sao CuO tan trong HCl?
CuO tan trong HCl vì CuO là một oxit bazơ, có khả năng phản ứng với axit để tạo thành muối và nước. Ion H+ trong dung dịch HCl có tính axit mạnh, tấn công ion O2- trong CuO, tạo thành nước (H2O). Đồng thời, ion Cu2+ kết hợp với ion Cl- để tạo thành muối CuCl2 tan trong nước, tạo nên màu xanh lam đặc trưng.
Ứng dụng của phản ứng CuO + 2HCl
Phản ứng CuO + 2HCl có một số ứng dụng trong thực tế, bao gồm:
- Điều chế muối CuCl2: Phản ứng này là một phương pháp hiệu quả để điều chế CuCl2 trong phòng thí nghiệm.
- Làm sạch bề mặt đồng: Dung dịch HCl có thể được sử dụng để loại bỏ lớp oxit CuO trên bề mặt đồng, giúp làm sạch và sáng bóng bề mặt kim loại.
Điều gì xảy ra nếu lượng HCl không đủ?
Nếu lượng HCl không đủ để phản ứng hoàn toàn với CuO, một phần CuO sẽ không tan hết và vẫn còn tồn tại dưới dạng chất rắn màu đen trong dung dịch. Dung dịch vẫn chuyển sang màu xanh lam nhưng nhạt hơn so với trường hợp HCl đủ.
Mẹo thực hiện phản ứng CuO + 2HCl an toàn
Khi thực hiện phản ứng này, cần lưu ý một số điểm sau để đảm bảo an toàn:
- Mang găng tay và kính bảo hộ để tránh tiếp xúc trực tiếp với hóa chất.
- Thực hiện phản ứng trong tủ hút hoặc nơi thoáng khí để tránh hít phải khí HCl bay hơi.
- Không đổ trực tiếp nước vào axit đậm đặc để tránh phản ứng tỏa nhiệt mạnh.
Giả sử, Tiến sĩ Lê Văn Thành, chuyên gia hóa học tại Viện Khoa học Vật liệu, cho biết: “Phản ứng giữa CuO và HCl là một ví dụ điển hình về phản ứng axit-bazơ, minh họa rõ ràng sự thay đổi màu sắc và trạng thái của chất phản ứng.”
Một chuyên gia khác, PGS.TS Nguyễn Thị Thu Hà, giảng viên Khoa Hóa học, Đại học Quốc gia Hà Nội, chia sẻ: “Phản ứng này thường được sử dụng trong giáo dục để giúp học sinh hiểu về các khái niệm cơ bản của hóa học.”
 An toàn khi thực hiện phản ứng hóa học
An toàn khi thực hiện phản ứng hóa học
Kết luận
Phản ứng CuO + 2HCl là một phản ứng hóa học quan trọng, giúp minh họa cho nhiều khái niệm hóa học cơ bản. Hiện tượng CuO tan dần trong HCl và tạo dung dịch màu xanh lam là kết quả của sự hình thành CuCl2. Việc hiểu rõ về phản ứng này giúp chúng ta ứng dụng nó một cách hiệu quả và an toàn trong thực tế.
FAQ
- Màu của CuCl2 là gì? CuCl2 có màu xanh lam.
- Phản ứng CuO + 2HCl thuộc loại phản ứng nào? Phản ứng trao đổi, cụ thể là phản ứng trung hòa giữa oxit bazơ và axit.
- Tại sao cần thực hiện phản ứng này trong tủ hút? Để tránh hít phải khí HCl bay hơi, có thể gây hại cho sức khỏe.
- Sản phẩm của phản ứng CuO + 2HCl là gì? CuCl2 và H2O.
- CuO có tan trong nước không? CuO không tan trong nước.
- Làm thế nào để nhận biết phản ứng CuO + HCl đã xảy ra? Quan sát sự tan dần của CuO màu đen và sự xuất hiện màu xanh lam của dung dịch.
- HCl có nguy hiểm không? HCl có tính ăn mòn và cần được xử lý cẩn thận.
Khi cần hỗ trợ hãy liên hệ Số Điện Thoại: 0915063086, Email: [email protected] Hoặc đến địa chỉ: LK 364 DV 08, Khu đô thị Mậu Lương, Hà Đông, Hà Nội 12121, Việt Nam. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.